中学生および高校の低学年生並びに大人でも文系の方々には、少し専門的な用語があって、難しく感じることがあると思われます。しかし、言葉に惑わされると話が先に進みませんから、判らない用語はそのままにして読みすすんでみてください。その後、解らない言葉や全体的な意味などは、周りにいる先生や先輩に教えてもらってください。
第一章 はじめに
私達の現代生活にはエネルギーが不可欠です。かつて生活に必要な要素は衣食住といわれました。今では医食住といったほうが良いかもしれませんが、現代社会はエネルギーを消費することを基盤としています。読者の皆さんは「エネルギー保存の法則」を知っていて、エネルギーは消えてなくならないので「消費する」という言い方は科学的には適切でないと考えるでしょう。
ここでこのエネルギーという言葉を身近な例で石油と置き換えてみます。まさに近代は石油を消費する時代で、発電、自動車用燃料、化学素材(繊維やプラスチック)などすべて

石油を燃料・原料として成り立っています。ですから世界中で起こっている紛争は石油資源確保のためといってもいいでしょう。
石油を代表とする化石燃料(他には石炭や天然ガスがある)を消費することで近年大きな課題がふたつ提起されています。一つは石油がなくなる、容易に入手できなくなるという問題です。中国やインドに代表される発展途上国の産業発展に伴って世界の石油消費量が急激に増大し、石油の生産・供給が近い将来間に合わなくなるのではないか、という懸念です。「ピークオイル」という言葉を聴いたことがあるでしょうか。これは石油の生産が消費に追いつかなくなり、石油生産量が減少してしまう状態のことを言います。このピークオイルが今後15年くらいの間に起こるという主張があります。
これに対しては、石油より資源量が多く世界中に分布している(したがって紛争の種にならない)石炭や天然ガス、あるいは非在来型資源と呼ばれるタールサンド(油を含んだ土)、シェールオイル(油を含んだ岩)、オリノコタール(粘度の高い油)、炭層メタン、メタンハイドレート(海底にある水の中のガス)の利用を進めるという方策があります。この様な新たな資源を開発・利用することでピークオイルがきても当面は大丈夫といえるかもしれません。しかし化石燃料が有限であることに変わりはありません。
もう一つの課題は地球温暖化です。化石燃料の燃焼により排出されるCO2を主原因として地表付近の気温が上昇し、北極の氷が解けて海面が上昇するという問題です。ここ数年で地球温暖化という言葉が良く聞かれるようになりましたが、20年以上前から大気中のCO2濃度増加による地球温暖化は指摘されていました。当時は原子力発電推進を目的に、火力発電を牽制するスローガンと認識されていましたが、1997年に京都議定書が議決されてから、世界中の問題としてあらゆる面で認識されるようになりました。
ところで私たちが身近に使っているエネルギーには、家のコンセント(電気)、自動車のガソリン、携帯電話のバッテリーなどがあります。最近、家庭用燃料電池システム、燃料電池自動車、小型機器用燃料電池という言葉を聴くことが増えました。日本では今現在約1300台の家庭用燃料電池と約30台の燃料電池自動車が実験的に使われています。本稿ではこれらの装置が研究開発される背景となるエネルギーの利用について考えてみます。
先にあげた二つの課題、すなわち石油供給の先行き不安と地球温暖化への対応策として、水素を利用するシステムすなわち水素社会の実現が叫ばれています。あるいは水素を燃料とする燃料電池を実用化することが解決策という主張があります。確かに燃料電池は直接には石油などの化石燃料を必要としませんし、それゆえCO2を直接排出しません。それでは燃料電池は地球温暖化と化石燃料の枯渇という課題を解決できるのでしょうか。
本稿の目的はこの質問に答えを示すことではありません。これらの問題を考える上で基本となるエネルギーや水素の役割を理解することです。
第二章 エネルギーとは何か
先に話を簡単にするためにエネルギー=石油としましたが、もちろんこれは正しい言い方ではありません。エネルギーにはいくつかの形態があるのを知っていますか。運動エネルギー、電気エネルギーや熱エネルギーは良く知られていますが、エネルギーといわれるからにはこれらに共通した特性、すなわちエネルギーの本質というものがあるはずです。
ここでもう一つのエネルギーの分類を理解しておく必要があります。一次エネルギーと二次エネルギーというわけ方です。エネルギーが保存されることを皆さんは知っています。逆に言えばエネルギーを無から作ることは出来ないわけですから、まず何らかの形態のエネルギーを自然界から持って来なければなりません。そしてこれを利用しやすい形の二次エネルギーに変換する必要があります。

この自然界から持ってくる最初のエネルギーが一次エネルギーです。水力は昔から利用されている一次エネルギーです。水車で臼を引く水車小屋や水力発電はその代表例です。風力や太陽光も一次エネルギーです。燃料に使う薪も自然界から取ってきますから一次エネルギーです。同様に石炭、石油、天然ガスも地中(自然界)から取ってくるので一次エネルギーといえます。
これに対して電気はどうでしょうか。雷は電気ですが、雷を直接電灯の電気に利用することは出来ません。水力や石油などの火力を利用して発電所で発電するわけですから、電気は二次エネルギーです。二次エネルギーは一次エネルギーから一度エネルギーの形態が変換されたものです。私達の生活では、ガスコンロや石油ストーブのように一次エネルギーをそのまま利用することもありますが、電気のように使い勝手の良い二次エネルギーを多く利用しています。
ところで水素そのものは石油と違って地中を掘っても出てくるものではありません。石油から水蒸気改質という方法で作ったり、電気で水を電気分解して作られるので、明らかに水素は二次エネルギーです。二次エネルギーとしての水素の利点は燃料電池により直接電気に変換できることですが、一次エネルギーの枯渇問題を二次エネルギーである水素利用により直接的に解決できないことは容易に理解できます。
さて物理化学では「エネルギーとは仕事をする能力」と定義します。運動する物体は別の物にぶつかれば弾き飛ばすという仕事をします。電気エネルギーはモーターでさまざまな仕事に変換されます。熱も蒸気機関車が走ることを考えれば、仕事をする能力を有していると理解できます。それではこれらのエネルギーはみんな同じと考えていいのでしょうか。
第三章 電熱器でお湯を沸かすのはもったいない?
(エネルギーの質と変換効率)
エネルギー保存の法則というのは、エネルギーの使用の前後でその形態が変わったり、いくつかに分かれたとしても全体の合計エネルギーは変わらないという「量」に関するものです。エネルギー保存の法則は熱力学の第一法則でもあります。
いま気温20℃の部屋に80℃のお湯1kgを置いておきます。時間が経てばお湯は冷めて20℃の水になります。このとき部屋に放出された熱エネルギーは
(80℃−20℃)×4.2kJ/kg/℃×1kg=252kJ
と計算されます。ここで4.2kJ/kg/℃というのは水の熱容量で、1kgの水の温度を1℃上昇させるのに必要な熱は4.2kJという意味です。
余談ですが数字に単位を付けて計算していることに注目してください。科学で扱う数値には必ず単位がつきます。この単位も合うように計算しなければいけません。逆に言うと単位を見れば割り算にするのか、掛け算にするのかが容易に分かるのです。
さて80℃より温度の低い50℃のお湯1kgならば部屋に放出される熱エネルギーは半分の126kJです。ですから50℃のお湯2kgを持ってくれば部屋に放出される熱エネルギーの量としては同じになります。ところで80℃のお湯と50℃のお湯は同じ仕事をする能力を有しているといえるでしょうか。高級なお茶は80℃くらいのお湯でいれて飲むものだそうです。筆者は安いお茶しか飲みませんので、おいしいかどうかは正直わかりません。しかし、50℃のお湯ではお茶を入れることはできません。
どうやら熱エネルギーには量のほかに質がありそうです。エネルギーの質は「エクセルギー」という量で表されます。エネルギーは仕事をする能力ですが、エクセルギーはそのうち有効に仕事に変換できる量といえます。上にあげた例から直感的に温度が高いとエクセルギーも高くなるということが理解できます。
エネルギーの形態がどう変化しても全部を合わせた総量は同じになることを先に説明しました。しかし、変換の過程には原理的に効率的なものとそうでないものがあります。他のエネルギーから熱エネルギーへの変換は簡単ですが、熱エネルギーから他の形態のエネ
ルギーへの変換は非効率で必ずエネルギーの損失が発生します。運動エネルギーは100%熱エネルギーに転換できます。ジュールという化学者がそのことを見出しました。電気エネルギーも原理的には100%仕事に変換することができます。
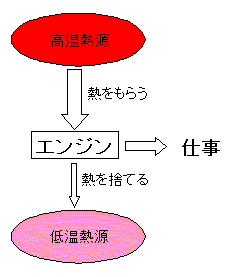
これらに対して、熱エネルギーを100%仕事に変換することはできません。カルノーという科学者が理想的な熱機関を考えましたが、彼はその中で熱を仕事に変える熱機関というものは必ず低温熱源に熱を捨てないと仕事が出来ないことを見出しました。これがカルノー効率といわれるもので
η=(Th−Tc)÷Th
で計算できます。ここでThは高温熱源の絶対温度、Tcは低温熱源の絶対温度です。カルノーのこの主張は熱力学の第二法則でもあります。
エネルギーの計算では温度に絶対温度を用います。絶対零度 0K(オーケーではなくゼロケルビンと読みます)=−273℃ を基準に考えます。どうして絶対温度を用いるのかを考えることは、温度とは何かを考えることになります。
例を挙げて考えてみます。50℃のお湯1kgに同じ50℃のお湯1kgを注ぎ足しました。重さは1kg+1kg=2kgになります。しかし温度は50℃+50℃=100℃にならないことを経験で知っていますが、それはどうしてでしょうか。それは、温度は熱の密度とみなせるからです。密度であればこれを足すことは出来ません。
もう少し詳しく説明しましょう。4℃の水の密度は1g/cm3です。これは4℃の水1cm3の重さを測ると1gあるということです。4℃の水100cm3ならば100gです。この4℃の水100cm3に同じ4℃の水100cm3を加えると、重さは200gになりますが、体積も200cm3になります。したがって密度は200g/200cm3=1g/cm3です。密度は足し算1g/cm3+1g/cm3=2g/cm3にはなりません。
温度が熱の密度とみなせるのであれば水の密度と同じように足し算は出来ません。大きなヤカンと小さなヤカンに水を入れ、同じガスコンロで同じだけ熱を加えたとします。小さなヤカンの方が温度は高くなると直感的に分かります。同じ熱を加えても水の体積が小さい分だけ熱はぎゅうぎゅうに詰め込まれるので熱の密度が大きくなり、その結果温度計で温度を測ると高い温度になっているのです。同じ体積の水の中に熱がたくさん入っていれば温度は高くなり、熱が少ししか入っていなければ温度は低くなります。
それではヤカンの水の中に全く熱が入っていない、つまり熱の密度がゼロだとしたらどうでしょうか。これが絶対零度です。熱の密度がゼロ、言い換えれば熱が全く無いのですからエネルギーゼロの状態です。エネルギー計算をするにはエネルギーゼロの状態を基準にする必要があるので、温度は0℃を基準にするのではなく絶対零度を基準にします。
話をカルノー効率に戻します。先の式からカルノー効率は低温熱源の温度が−273℃でないと100%になりません。部屋の温度を−273℃に保っておくことは出来ませんから、熱を仕事に変えようとすると効率は必ず100%よりも低くなります。そうであれば熱エネルギーは他の形態のエネルギーに比べて価値が低いということになります。エネルギーの価値は仕事をする能力ですから、この基準でエネルギーの形態に順序を付けると、電気と力学的エネルギーが一番、次が化学エネルギーで熱は最も低いことになります。そして熱の中でも温度の低いものほど順番が低い、つまり価値が低いというわけです。電気は一番価値の高いエネルギーですから、二次エネルギーとして電気を作ることは理にかなっているのです。
ここで電熱器でお湯を沸かすことを考えてみます。電熱器を使えば電気エネルギーを簡単に熱エネルギーに変えることができます。電熱器の温度はだいたい800℃くらいになります。室温を20℃とすると、この電熱器のカルノー効率は
η=((800+273)K−(20+273)K)÷(800+273)K=72.7% です。

電熱器で電気エネルギーを熱エネルギー(ジュール熱という)に変えた瞬間に、27.3%ものエネルギーを仕事に変換できない熱エネルギーとして部屋の中に捨てたことになります。
さらに20℃の水を100℃のお湯にするのに必要な熱量は
q=(100℃−20℃)×4.2kJ/kg/℃×1kg=336kJ です。
電熱器の加熱効率を80%(残りの20%はヤカンに伝わらず部屋の空気に逃げていく)とすると、電熱器は
w=336kJ÷0.8=420kJ=0.117kWh
の仕事をしたことになります。電熱器が何かを持ち上げるような仕事をするわけではありませんが、仕事=熱ですからこう表現します。
一方、室温20℃のときに100℃の物体が持つ熱エネルギーの「エクセルギー」は、熱エクセルギー比の一覧表を調べると0.1158と分かります。つまり100℃のお湯の持つエクセルギーは
ex=336kJ×0.1158=38.9kJ
と計算できます。電熱器は水のエクセルギーをたった38.9kJ上げるために420kJもの仕事を投入したことになり、電熱器の仕事の効率はわずか9.3%です。電熱器でお湯を沸かすことがいかに非効率であるかがわかります。
電気エネルギーを使って風呂や台所のお湯を沸かすためにはヒートポンプを使用することがエネルギー効率的には推奨されます。ヒートポンプは熱を運ぶ機械です。
川の水は高い所から低い所に流れます。この水を低い所から高い所に移動させるにはポンプを使います。重力に逆らって水を移動させるのでポンプは仕事をします。熱も自然には高温から低温に向かって移動します。ヒートポンプは電気で圧縮機を回す仕事をして、低温から高温に熱を移動させる機械です。家庭のエアコンは、夏には涼しい部屋から暑い外気に熱を移動させ、冬には逆に寒い外気から暖かい部屋の中に熱を移動させます。電気を熱に変換するのではなく、熱を移動させるという仕事を電気で行なっているので、仕事の3倍もの熱量を移動させることが出来ます。単純に効率を計算すると300%です。但し、100%を上回るからといってエネルギーが増えるわけではありません。
さて水素エネルギーはどうでしょうか。正確には水素の持つ化学エネルギーの質は良いのでしょうか、悪いのでしょうか。次はこのことを考えてみます。
第四章 燃料電池はなぜ注目されているのか?
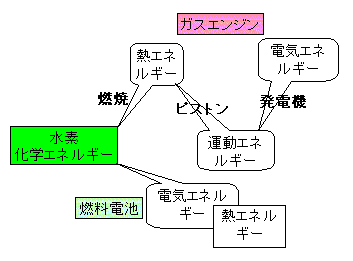
燃料電池は乾電池の一種ではなく発電機です。水素を燃料とするため排出ガスはH2Oだけです。温室効果ガスの大部分を占めるCO2を排出しないためクリーンな装置といわれることもあります。しかし水素を燃料にガスエンジンを利用しても発電は可能で、排出ガスは原則としてH2Oだけです。燃料電池が注目されるのはCO2を排出しないクリーンな装置だからというだけではありません。
燃料電池が科学者たちから注目されたのはその発電効率が高いからです。ガスエンジンも燃料電池も水素が酸化されて水に変わるときの化学エネルギー変化をもとに発電しますが、その機構は少々異なります。以下ではいくつかの専門用語を用います。燃料電池とガスエンジンの発電効率を比較するにはどうしても必要なものですが、専門的なので一つ一つの用語の説明はごく簡単にします。
物理化学という学問は化学エネルギーと仕事の量的関係を教えてくれます。式にあらわすと
ΔH=ΔG+TΔS です。
Hはエンタルピーと呼ばれる量で、物質の持つ内部エネルギーと圧力・体積でその値が決まります。Δは変化して増えたり減ったりした量を表しますが、ΔHは燃焼前と燃焼後の差、簡単に言えば燃焼により発生する熱量です。Gはギブスの自由エネルギーと呼ばれる量で、ここでは仕事を表します。Tは絶対温度です。Sはエントロピーと呼ばれる量で熱力学の計算をするうえでは重要な値です。気体を圧縮すると温度が上がります。自転車の空気入れが熱くなるのを経験したことがあるでしょう。空気を圧縮した時、空気入れの温度が上がらないように放熱させたとします。この時放熱した熱量をQ、その時の温度をTとするとΔS=Q/Tで計算されます。ですからTΔS=T×(Q/T)=Qとなり、TΔSは熱を表します。この式は、水素の持つ化学エネルギーは仕事と熱になり、しかもその量的関係はこうだと教えてくれます。
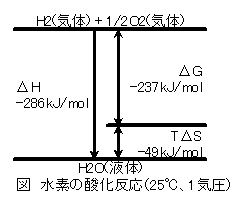
次の図は25℃、1気圧の条件下でこの反応が進行したときのエネルギーに関わる変化を表す数値です。これらの数値は化学便覧で知ることができます。燃料電池で発電(仕事)に変換できる量はΔGです。そうすると発電の理論効率は
η=ΔG÷ΔH
ですから、
(−237kJ/mol)÷(−286kJ/mol)=82.9%
(ここでmolは水素ガス1モルを指します)
になります。それぞれの数値にはマイナスの符号がついています。物理化学では注目している系に与えられる熱量を正と定義します。ここでは上から下(水素と酸素から水が生成する)への反応は熱放出をするので負の符号を付けて表します。ここで反応が25℃、1気圧で進行していることが重要です。温度が高くなるとTΔSの値が大きくなってしまいますから、ΔGの値すなわち発電量が小さくなってしまい、発電効率は低下します。
一方、ガスエンジンによる発電では水素が燃焼してその燃焼熱により作動流体を膨張させピストンを動かして発電機を回します。燃焼温度は最高で2,000℃にも達しますのでTΔSの値は大きくなり、ΔGの値は著しく小さくなります。このような熱機関による仕事の効率はカルノー効率が最大になることは先に説明しました。
一般的なガソリンエンジンでは60℃、1気圧の作動流体を15気圧程度まで圧縮します。断熱圧縮されたガスの温度は449℃になります(どうしてこの温度になるのかの計算・説明は省きます)ので、カルノー効率は
η=((449+273)K−(60+273)K)÷(449+273)K=53.9%
と計算されます。先に説明した熱力学の第二法則が教えてくれるところでは、熱を仕事に変えるには低温熱源に熱を捨てる必要があるわけで、熱の全量を仕事に変えることはできません。したがって発電効率も低くなるのです。
摩擦や放熱ロスがまったくないとして比較すると、燃料電池の発電効率82.9%、熱機関は53.9%ですからは熱機関に比べて格段に高いことがわかります。したがってこの原理から考えて燃料電池の発電効率は現状利用している熱機関発電機(発電所)に比べて高くできると科学者は期待したのです。
それでは燃料電池の発電効率をもっと高くすることは理論的に可能でしょうか。
先のΔH=ΔG+TΔSの式から考えれば、ΔSつまりエントロピー変化の小さい反応、酸化された時にエントロピー変化の小さい物質を選べば良いことがわかります。
その一例を示します。
C(固体)+O2(気体)−>CO2(気体)
の反応ではΔS=−2.86J/mol/Kですから25℃ではTΔS=−0.8kJ/molです。これより効率を計算すると
(−394kJ/mol−(−0.8kJ/mol))÷(−394kJ/mol)=99.8% です。
つまり炭素を燃料とする燃料電池ができればほぼ100%の発電効率が得られることになります。しかし25℃という温度で炭素が酸化されないことを私たちは日常の経験から知っています。バーベキュー用の炭を倉庫に置いておいたら一ヶ月で酸化されて無くな

った、などということは起こりません。この反応は直ぐには実現しそうもありません。それでも将来25℃で炭素を酸化させる触媒を見出すことができれば、効率100%の燃料電池も夢ではありません。
これまでは理想的な装置や理論効率を考えてきましたが、実際に装置を作って稼動させた時には摩擦や放熱、電気抵抗といったエネルギー損失があります。都市ガスやプロパンガスを燃料にして稼動している実際の家庭用燃料電池では、発電効率約30%、熱回収効率約40%です。理論効率からは大分小さくなっています。コンセントの電力、つまり大規模発電所の発電効率は37%(受電端効率)ですから、燃料電池のほうが発電効率は低くなっています。
一般に装置は小型になると効率が下がる傾向があります。損失のうち最も大きなものは放熱ロスです。放熱は(熱伝導度)×(温度差)×(放熱面積)で計算されます。大規模な装置では体積あたりの表面積つまり放熱面積が小さくなるので、熱ロスが減少し効率が高くなります。発電所や化学工場などの装置が大型なのは、その方が効率的に有利だからです。
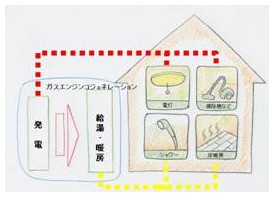
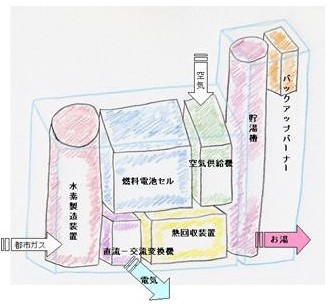
しかし燃料電池はその原理から化学エネルギーを直接電気エネルギーに変換し、熱の発生を頼りにしません。ですから小規模でも効率が下がることはありません。さらに小規模にすることで家庭におくことができます。そうすると排熱を回収してこれでお湯を沸かす(お風呂や暖房用)ことができます。電気と熱の両方を利用することができるので、このような装置をコジェネレーションといいます。左の図はガスエンジンを利用した家庭用コジェネレーションシステムです。コジェネレーションの総合効率は発電効率と熱効率の足し算ですから、先の家庭用燃料電池は70%の効率となります。
これに対して、大規模発電所の排熱で例えば大きな銭湯を作っても、わざわざ遠くの発電所まで風呂に入りにいく人はいません。結局発電所の熱エネルギーは川の水や海水に捨てられるだけなのです。
現在の小型の燃料電池は大規模発電所に比べて発電効率では劣るかもしれませんが、総合効率では間違いなく勝ります。さらに、水素燃料電池の理論効率は高いですから、これからどんどんと装置が改良されれば、発電効率でも大規模発電所をしのぐことが予想されます。このように燃料電池が注目されているのは、発電効率が高く、その上CO2を排出しないからです。
 iPodや携帯電話は必ずしも社会生活に必要不可欠というものではありませんが、心臓ペースメーカーに入っている電池などは直接命に関わるほど重要なものです。電気エネルギーは大量に安定的に、安全に、効率よく作ることが大事ですが、効率が悪くてもエネルギー密度が高ければ良いという使い道もあります。つまり、大量に効率よくエネルギーを作る技術と少量でも高密度に貯めておく技術は、それぞれ目的が違いますから同じ土俵で比較しても意味がありません。
iPodや携帯電話は必ずしも社会生活に必要不可欠というものではありませんが、心臓ペースメーカーに入っている電池などは直接命に関わるほど重要なものです。電気エネルギーは大量に安定的に、安全に、効率よく作ることが大事ですが、効率が悪くてもエネルギー密度が高ければ良いという使い道もあります。つまり、大量に効率よくエネルギーを作る技術と少量でも高密度に貯めておく技術は、それぞれ目的が違いますから同じ土俵で比較しても意味がありません。
 「主な対象読者」
「主な対象読者」
 石油を燃料・原料として成り立っています。ですから世界中で起こっている紛争は石油資源確保のためといってもいいでしょう。
石油を燃料・原料として成り立っています。ですから世界中で起こっている紛争は石油資源確保のためといってもいいでしょう。



 この自然界から持ってくる最初のエネルギーが一次エネルギーです。水力は昔から利用されている一次エネルギーです。水車で臼を引く水車小屋や水力発電はその代表例です。風力や太陽光も一次エネルギーです。燃料に使う薪も自然界から取ってきますから一次エネルギーです。同様に石炭、石油、天然ガスも地中(自然界)から取ってくるので一次エネルギーといえます。
この自然界から持ってくる最初のエネルギーが一次エネルギーです。水力は昔から利用されている一次エネルギーです。水車で臼を引く水車小屋や水力発電はその代表例です。風力や太陽光も一次エネルギーです。燃料に使う薪も自然界から取ってきますから一次エネルギーです。同様に石炭、石油、天然ガスも地中(自然界)から取ってくるので一次エネルギーといえます。
 いま気温20℃の部屋に80℃のお湯1kgを置いておきます。時間が経てばお湯は冷めて20℃の水になります。このとき部屋に放出された熱エネルギーは
いま気温20℃の部屋に80℃のお湯1kgを置いておきます。時間が経てばお湯は冷めて20℃の水になります。このとき部屋に放出された熱エネルギーは
 ルギーへの変換は非効率で必ずエネルギーの損失が発生します。運動エネルギーは100%熱エネルギーに転換できます。ジュールという化学者がそのことを見出しました。電気エネルギーも原理的には100%仕事に変換することができます。
ルギーへの変換は非効率で必ずエネルギーの損失が発生します。運動エネルギーは100%熱エネルギーに転換できます。ジュールという化学者がそのことを見出しました。電気エネルギーも原理的には100%仕事に変換することができます。



 η=ΔG÷ΔH
η=ΔG÷ΔH
 った、などということは起こりません。この反応は直ぐには実現しそうもありません。それでも将来25℃で炭素を酸化させる触媒を見出すことができれば、効率100%の燃料電池も夢ではありません。
った、などということは起こりません。この反応は直ぐには実現しそうもありません。それでも将来25℃で炭素を酸化させる触媒を見出すことができれば、効率100%の燃料電池も夢ではありません。